실험 개요
촉매는 반응 전과 후에 거의 그대로 남으면서, 반응이 더 빠르게 진행되도록 돕습니다.
관찰 포인트
- • 촉매 조건을 바꾸면 거품이 솟는 속도가 달라집니다.
- • 반응이 빠를수록 열도 함께 더 뚜렷하게 느껴집니다.
- • 농도가 높을수록 변화가 크게 보일 수 있습니다.
원리 한 줄 정리
촉매는 반응 경로를 바꾸어 활성화 에너지를 낮추고, 그 결과 같은 조건에서도 반응이 더 빨라집니다.
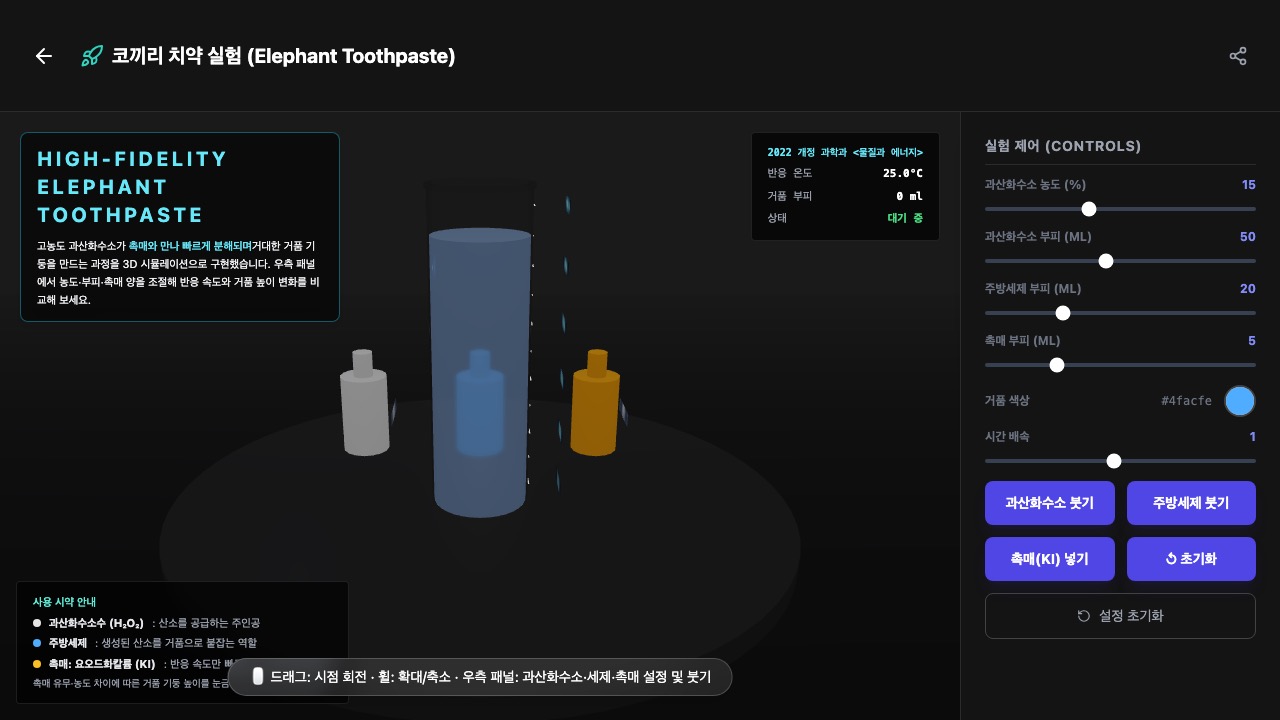
촉매가 반응 속도를 키우는 거품 기둥 실험
과산화수소 분해 반응이 빠르게 일어나며 거품과 열이 생기는 모습을 안전하게 관찰합니다.
기술 스택
canvas2d
태그
촉매 · 발열 · 과산화수소
커리큘럼
2022 개정 화학 · 반응 속도
릴리즈
2026-04-22
촉매는 반응 전과 후에 거의 그대로 남으면서, 반응이 더 빠르게 진행되도록 돕습니다.
촉매는 반응 경로를 바꾸어 활성화 에너지를 낮추고, 그 결과 같은 조건에서도 반응이 더 빨라집니다.
실험 시작
과산화수소 분해 반응이 빠르게 일어나며 거품과 열이 생기는 모습을 안전하게 관찰합니다.
Related